在人體腸道內,棲息著像乳酸菌等數萬億微生物,它們不僅協助消化食物,更在免疫系統塑造中扮演關鍵角色。這些微生物通過釋放各類分子與宿主“對話”,調控免疫細胞的生長與功能。不過,在如此復雜的微生物群落中,宿主能否在“茫茫菌海”中選擇性識別并管理特定細菌?
來自上海的科學家有了最新發現。5月14日晚,在《自然》期刊發表的一項研究中,中國科學院上海營養與健康研究所錢友存研究組,聯合中國科學院分子細胞科學卓越創新中心宋昕陽研究組成功破解了這一難題,揭示了一種宿主與腸道菌群互作的新機制。
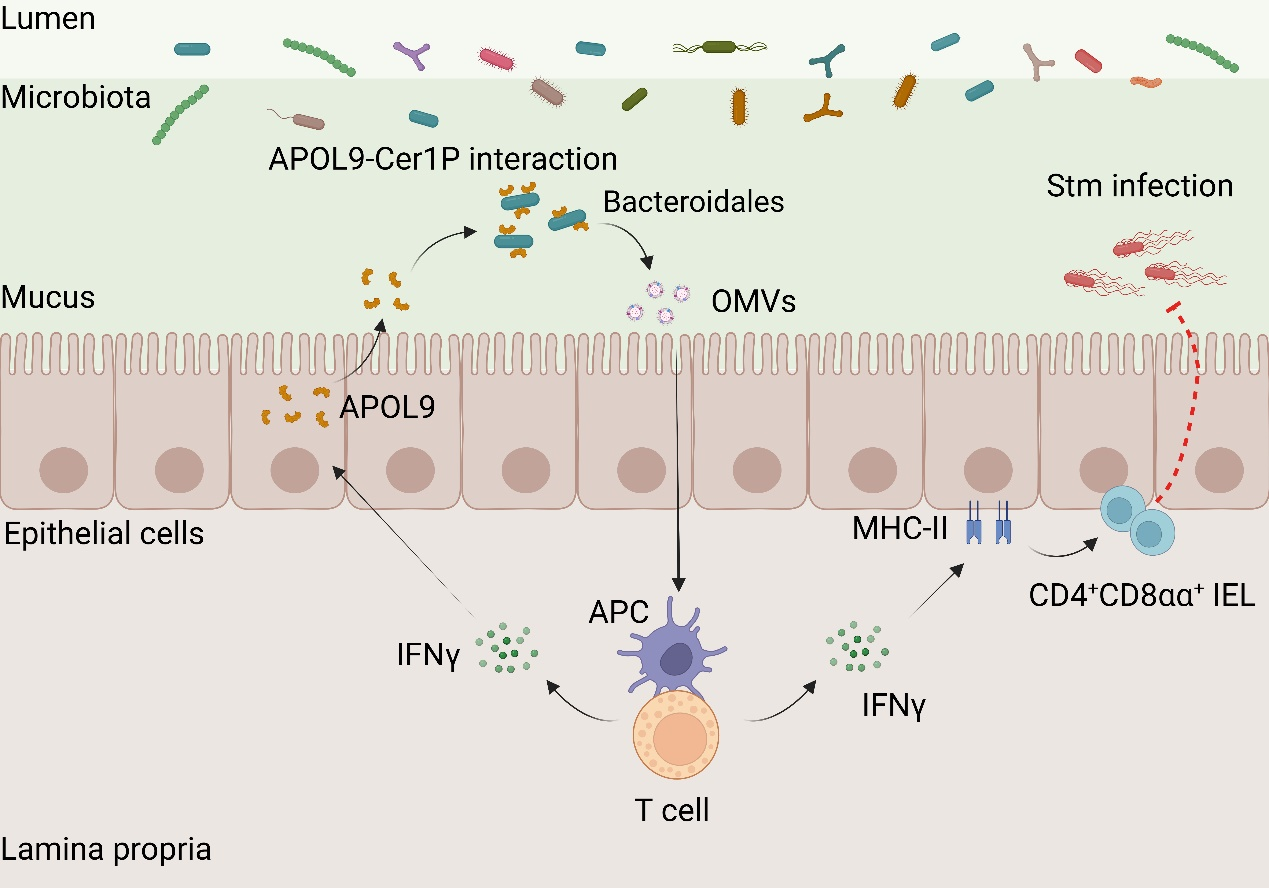
圖:新型載脂蛋白APOL9通過結合擬桿菌Cer1P分子誘導OMVs釋放并激活IFN-γ-MHC-II通路以增強腸道黏膜免疫,采訪對象提供
他們發現小鼠腸道上皮細胞會分泌一種“智能識別器”——APOL9蛋白(在人類中對應APOL2)。這種蛋白能夠精準識別一類擬桿菌目細菌,機制就如同“掃描儀讀取條形碼”一般,專門識別其細胞膜上的特殊脂質“標記”。
這項研究再次證明,腸道不僅是消化吸收的場所,更是宿主與微生物共同編織的精密免疫網絡的核心。破譯其中的分子密碼,將為人類健康帶來深遠影響。APOL9如同一位訓練有素的“細菌外交官”,與特定細菌建立精細化合作,助力維持腸道免疫穩態。“該研究首次證實,宿主能通過細菌特征性脂質標記,實現選擇性‘身份識別’。”錢友存告訴第一財經記者。
調節菌群或可像鋼琴調音
如果你喜歡酸奶,想必對乳酸菌等益生菌并不陌生。但實際上,它們只是腸道中龐大微生物群的一小部分。早在人類誕生前,這些微生物便與我們的祖先攜手進化,結成了密不可分的共生聯盟。除了輔助食物消化和營養吸收外,它們通過釋放代謝產物(如短鏈脂肪酸)與機體免疫系統“對話”。而機體則通過腸道上皮——這道細胞構成的“長城”——部署黏液屏障盾牌、抗菌蛋白武器等“防御系統”,與菌群協同維持生態平衡,使它們在各自的“領地”中穩定生存。

采訪單位供圖
這次發現的這個名為APOL9的蛋白有多神奇?研究團隊解釋,它具備“定點溝通”的能力——就如同一位訓練有素的“細菌外交官”,與特定細菌建立精細化合作,助力維持腸道免疫穩態。“或許在未來,調節菌群將如同鋼琴調音一般精細可控”。
宋昕陽補充解釋,APOL9并不直接殺菌,而是促使細菌釋放大量納米級“信息膠囊”——即外膜囊泡(OMVs),作為與機體溝通的信使。樹突狀細胞捕獲OMVs后激活免疫反應,增強“警報系統”——MHC-II分子的表達,推動一類特殊免疫細胞的發育,從而顯著提升腸道對有害菌的防御能力。
這項突破性研究首次闡明:宿主蛋白可通過識別細菌脂質標志物,觸發有益的免疫反應;同時揭示了一種主動塑造菌群的新范式——宿主并非被動容忍微生物,而是可以通過主動的分子“對話”實現腸道微生態的動態平衡。該發現為開發"菌群-免疫"協同調控的下一代療法開辟了新路徑。
北京大學基礎醫學院教授、博士生導師姜長濤點評說,腸道菌群與宿主的交互調控及對疾病的影響一直是領域研究熱點,但宿主基因如何調控菌群的機制仍有待挖掘。上述研究顛覆了傳統抗菌蛋白直接殺菌的認知范式,為腸道感染、炎癥性腸病等疾病的治療提供了新思路。此外,人源APOL2的功能保守性提示該機制可能具有跨物種普適性,為轉化醫學研究奠定基礎。
清華大學基礎醫學院教授、博士生導師胡小玉教授點評該研究時認為,宿主與腸道微生物的共生平衡對維持機體健康至關重要,其失衡與炎癥性腸病、代謝綜合征等慢性疾病密切相關。腸道上皮細胞作為宿主與微生物接觸的首道屏障,不僅構成物理阻隔,還通過分泌多種功能蛋白調節菌群結構和功能。研究所揭示的“APOL9a/b-Cer1P-OMVs-IELs”免疫調控軸,為未來針對腸道微生物組失衡相關疾病的精確干預提供了新思路和潛在靶點。
十余年的攻關
從錢友存、宋昕陽(兩位為共同通訊作者)再到楊濤(共同第一作者),這個由師徒同門合力研究11年的課題也是營養與健康所“揭榜掛帥”重大科技任務的成果之一。
2015年,楊濤剛入讀博士,與即將畢業的師兄宋昕陽一起投入到該項工作中。2016年,宋昕陽去哈佛醫學院從事博士后研究,并于2021年回國,入職同在岳陽路320號大院內的中國科學院分子細胞科學卓越創新中心。
2021年11月,營養與健康所整合組建實行計劃單列五周年之日,研究所舉行“十四五”期間首批重大科技任務“揭榜掛帥”啟動會,錢友存研究員領銜的“腸道免疫重塑及轉歸”就是重大科技任務之一,與所里4位年輕研究組長形成攻關團隊,當時即獲得所長基金啟動資助,并實行“包干制”等放權模式。嘗試“首席科學家 研究員”的團隊協同模式。
“在岳陽路320號讀博的這個期間其實就感受到了這個大院的創新氛圍,所以博士后回來后,再去選擇去哪家單位的時候,只面試了這里,不僅可以找到各個學科的科學家來合作,領域內的科研平臺也是全國最好的,所以回來的決定做得非常快。”宋昕陽說。
回國后,宋昕陽和錢友存研究員團隊合作,繼續上述研究,博士后階段的學習經歷也讓他們的研究有了快速進展。2022年,他們就發現APOL9通過結合細菌表面的一種特殊脂質分子識別擬桿菌。
“科研往前走是伴隨著技術進步的,10年前我們剛開始做的時候是和師弟楊濤一起發現的,但關于研究機制的問題擱置就出國了。”博士后階段學習了先進的微生物編輯技術后,也讓宋昕陽對腸道微生物的理解更深,他說,科研就是像是一條迂回前進的路徑,“再把這個問題翻回來看,很多東西就一目了然了。”
幫企客致力于為您提供最新最全的財經資訊,想了解更多行業動態,歡迎關注本站。鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播更多信息之目的,如作者信息標記有誤,請第一時間聯系我們修改或刪除,多謝。



